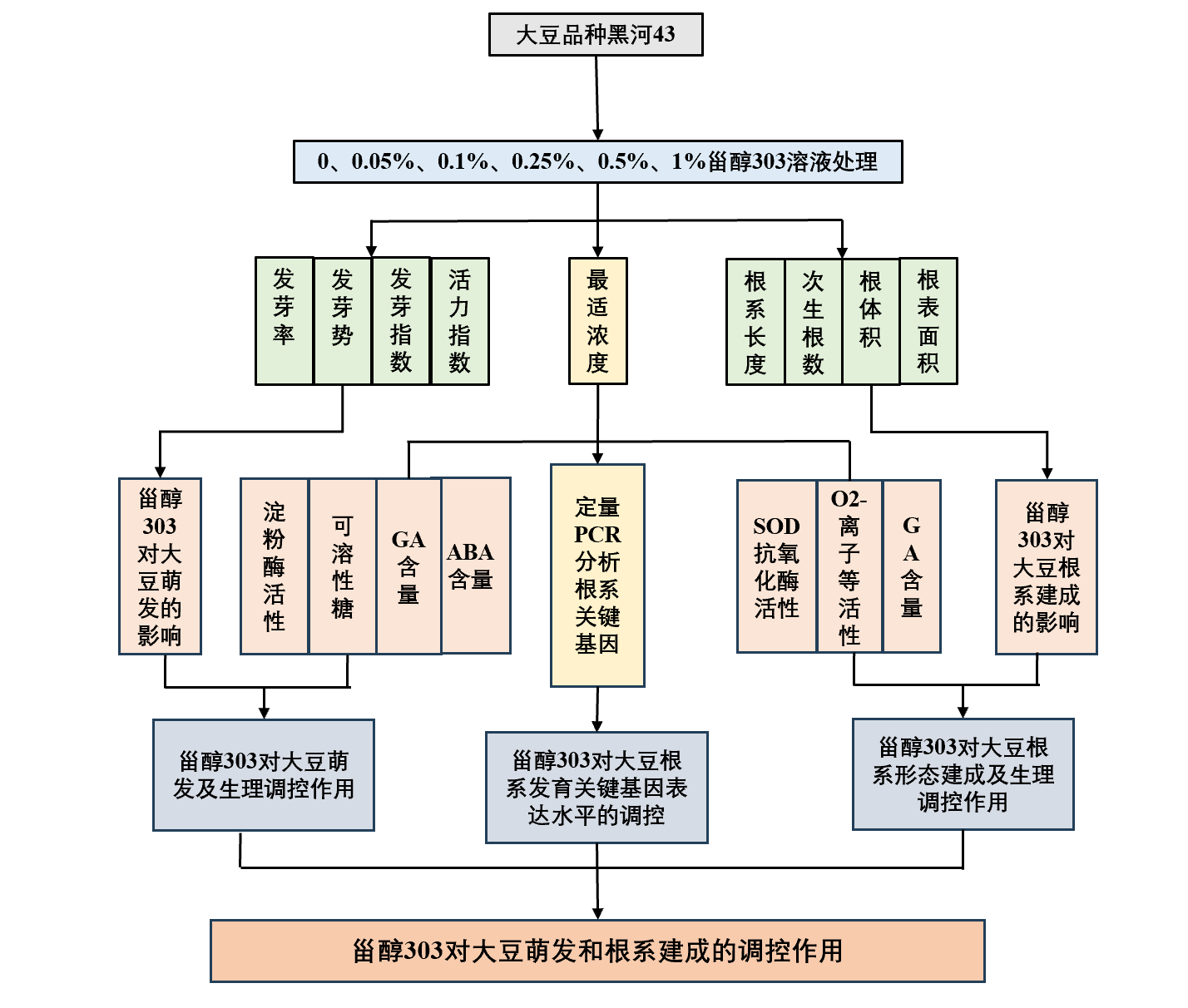
1.植物生长调节剂对大豆种子萌发的调控
萌发是种子形态和生理发生一系列有序变化的过程,实质是胚的活化、生长和储存营养的转化、运输。在调控萌发的众多机制中激素平衡(自然条件下植物自身和土壤细菌均会产生激素)是非常重要的一个方面。
通过改变内源激素平衡可调控大豆种子萌发,例如利用ABA拮抗剂[1]和GA合成抑制剂[2]处理大豆种子,可分别起到促进和抑制大豆种子发芽势的作用,究其原因是分别提高和降低了GA/ABA比值。外源生长素能够促进ABA合成的同时抑制GA合成,进而降低GA1/ABA和GA4/ABA的比值,导致大豆种子萌发受到抑制[3]。外源乙烯处理可在一定程度上提高赤霉素水平,并抑制生长素和脱落酸生物合成和信号转导,显著提高大豆发芽率[4]。采用乙酰半胱氨酸处理大豆种子则会抑制胚轴中乙烯生物合成,并降低H2O2含量,导致萌发受阻,外源乙烯或H2O2可解除乙酰半胱氨酸的抑制作用[5]。另外,适宜浓度的水杨酸[6]复硝酚钠[7]和壳聚糖[8]均可促进大豆种子萌发。进一步转录组学研究表明,大豆种子萌发期间脱落酸途径受到抑制,赤霉素、乙烯和油菜素类固醇途径上调[9]。
种子老化和逆境胁迫是生产中限制大豆萌发的重要因素,DA-6处理老化大豆种子可上调转化酶相关基因表达,促进三酰甘油的水解和脂肪酸向糖的转化,提高吸胀过程中可溶性糖的浓度,促进萌发[10]。盐胁迫下GA1/ABA、GA3/ABA和GA4/ABA等比率降低[11],大豆种子萌发受阻,适宜浓度的SA可显著提高NaCl胁迫下大豆种子活力,促进萌发和幼苗生长[12]。另外,适宜浓度的褪黑素可在一定程度上缓解盐胁迫[13]、干旱[14]和低温[15]对大豆萌发的不利影响。
2.植物生长调节剂对大豆根系表型特征的调控
根系具有机械固定、吸收水分和养分的功能,同时可感知土壤理化参数和微生物信息,协调植株整体生长发育。根系结构特征与功能密切相关,并受包括乙烯、生长素、脱落酸、赤霉素、细胞分裂素、茉莉酸和油菜素多种激素调控[16]。大豆根系特征与共生固氮、产量关系密切[17],因此通过植物生长调节剂调控大豆根系表型有望促进养分吸收和生物固氮能力,进而提高产量。
室内研究表明,低浓度IAA处理大豆幼苗能够促进主根伸长生长和侧根发育,而IBA、NAA和高浓度IAA则起抑制作用[18]。低浓度ABA处理对大豆根系表型无影响,高浓度则显著抑制了主根伸长和侧根数量,导致根系总长度显著降低;低浓度GA3可促进总根长增加,高浓度则起抑制作用[19]。6-BA对根系表型也有调控作用,且表现为明显的浓度效应[20]。大田试验表明,在V7期喷施冠菌素可显著提高根系生物量,并促进根系中分裂素和脱落酸含量提高,降低脱落酸含量[21]。另外,烯效唑和DA-6浸种[22, 23]、V3期叶面喷施水杨酸[24]均可促进大豆根系生长。另外,烯效唑可显著增加套作下大豆根长、根体积和根干重[25]。众多研究认为,外源PGR对根系形态特征的调控是通过改变内源激素如IAA、ABA等实现的[23,
26,27]。
阶段性干旱和涝害是造成大豆减产的主要逆境胁迫,其中主要原因主要是限制了大豆根系发育。梁晓燕研究表明,通过烯效唑浸种可显著促进旱胁迫下大豆幼苗根系发育,提高根系总根长和根表面积等根系形态指标[28]。水杨酸和茉莉酸同样可缓解干旱胁迫对大豆根系生长的不利影响,促进植株生长[29]。乙烯可促进淹水胁迫下大豆不定根数量的增加,提高根系表面积[30]。褪黑素则具有恢复淹水大豆根部木质化的作用[31]。
参考文献:
[1] Song D, Zhou J, Lai L, et al. Development of
ABA Antagonists to Overcome ABA-and Low Temperature-Induced Inhibition of Seed
Germination in Canola, Lentil, and Soybean[J]. Journal of Plant Growth
Regulation, 2019: 1-11.
[2] Gazara R K, Oliveira E A G D, Rodrigues B C,
et al. Transcriptional landscape of soybean ( Glycine max ) embryonic axes
during germination in the presence of paclobutrazol, a gibberellin biosynthesis
inhibitor[J]. Scientific Reports, 2019, 9(1):9601.
[3] Shuai H, Meng Y, Luo X, et al. Exogenous
auxin represses soybean seed germination through decreasing the
gibberellin/abscisic acid (GA/ABA) ratio[J]. Scientific reports, 2017, 7(1):
1-11.
[4] Manoharlal R, Saiprasad G V S. Assessment of
germination, phytochemicals, and transcriptional responses to ethephon priming
in soybean [Glycine max (L.) Merrill][J]. Genome, 2019, 62(12): 769-783..
[5] Ishibashi Y, Koda Y, Zheng S H, et al.
Regulation of soybean seed germination through ethylene production in response
to reactive oxygen species[J]. Annals of Botany, 2013, 111(1): 95-102.
[6] 刘小阳.
不同浓度的JA对大豆种子萌发和幼苗生理的影响[J]. 宿州学院学报, 2013, 28(12):90-92.
[7] 于彩莲,
刘波, 燕红,
等. 复硝酚钠及其组分对大豆种子萌发的影响[J]. 大豆科学, 2010, 29(03):440-443.
[8] Hai N T T, Thu L H, Nga N T T, et al.
Preparation of Chitooligosaccharide by Hydrogen Peroxide Degradation of Chitosan
and Its Effect on Soybean Seed Germination[J]. Journal of Polymers and the
Environment, 2019, 27(9):2098-2104.
[9] Bellieny-Rabelo D, De Oliveira E A G, da
Silva Ribeiro E, et al. Transcriptome analysis uncovers key regulatory and
metabolic aspects of soybean embryonic axes during germination[J]. Scientific
reports, 2016, 6(1): 1-12.
[10] Shu K, Qi Y, Chen F, et al. Salt stress
represses soybean seed germination by negatively regulating GA biosynthesis
while positively mediating ABA biosynthesis[J]. Frontiers in plant science,
2017, 8: 1372.
[11] Xu X, Fan R, Zheng R, et al. Proteomic
analysis of seed germination under salt stress in soybeans[J]. Journal of
Zhejiang University Science B, 2011, 12(7): 507-517.
[12] 倪祥银,
齐泽民, 廖姝,
等. 外源水杨酸对NaCl胁迫下大豆种子萌发和幼苗生长生理的影响[J]. 西北植物学报, 2014, 34(01): 106-111.
[13] 王明瑶,
曹亮, 于奇,
等. 褪黑素浸种对盐碱胁迫下大豆种子萌发的影响[J]. 作物杂志,
2019, (06): 195-202.
[14] 秦彬,
张明聪, 何松榆,
等. 褪黑素浸种对大豆种子萌发过程中干旱胁迫的缓解效应[J]. 干旱地区农业研究, 2020, 38(02): 192-198.
[15] 于奇,
曹亮, 金喜军,
等. 低温胁迫下褪黑素对大豆种子萌发的影响[J]. 大豆科学, 2019, 38(01): 56-62.
[16] Qin H, He L, Huang R. The coordination of
ethylene and other hormones in primary root development[J]. Frontiers in plant
science, 2019, 10: 874.
[17] Yang Y, Zhao Q, Li X, et al. Characterization
of genetic basis on synergistic interactions between root architecture and
biological nitrogen fixation in soybean[J]. Frontiers in plant science, 2017,
8: 1466.
[18] 李欣欣,
赵静, 廖红.
吲哚乙酸、吲哚丁酸和萘乙酸对大豆幼根生长的影响[J]. 植物生理学报, 2013, 49(06): 573-578.
[19] 李欣欣,
廖红, 赵静.
GA3、ABA和6-BA对大豆根系生长的影响[J]. 华南农业大学学报, 2014, 35(03): 35-40.
[20] Rahdari P, Sharifzadeh V. Effects of Auxin and
Cytokinin on morphological and Physiological factors in Soybean (Glycin max
L)[J]. Life Sci. J, 2012, 9: 5796-5807.
[21] Shen X, Chen Y, Li J, et al. Coronatine effects
on yield, nutrient uptake, and physio-biochemical attributes of soybean
roots[J]. Journal of Plant Nutrition, 2018, 41(5): 664-671.
[22] 冯乃杰,
阎秀峰, 郑殿峰,
等. 两种植物生长调节剂浸种对大豆根系解剖结构的影响[J]. 植物生理学通讯, 2010, 46(07): 687-692.
[23] Han Y, Gao Y, Shi Y, et al. Genome-wide
transcriptome profiling reveals the mechanism of the effects of uniconazole on
root development in Glycine Max[J]. Journal of Plant Biology, 2017, 60(4):
387-403.
[24] Gutiérrez-Coronado M A, Trejo-López C,
Larqué-Saavedra A. Effects of salicylic acid on the growth of roots and shoots
in soybean[J]. Plant Physiology and biochemistry, 1998, 36(8): 563-565.
[25] Yan W, Yanhong Y, Wenyu Y, et al. Responses of
root growth and nitrogen transfer metabolism to uniconazole, a growth
retardant, during the seedling stage of soybean under relay strip intercropping
system[J]. Communications in soil science and plant analysis, 2013, 44(22):
3267-3280.
[26] Prince S J, Valliyodan B, Ye H, et al.
Understanding genetic control of root system architecture in soybean: Insights
into the genetic basis of lateral root number[J]. Plant, cell &
environment, 2019, 42(1): 212-229.
[27] Han Y Q, Shi Y, Gao Y M, et al. Treatment of
Glycine max seeds with gibberellins alters root morphology, anatomy, and
transcriptional networks[J]. Biologia Plantarum, 2020, 64:32-42.
[28] 梁晓艳.
烯效唑对干旱胁迫下苗期大豆根系的调控[D]. 黑龙江八一农垦大学, 2019.
[29] Mohamed H I, Latif H H. Improvement of drought
tolerance of soybean plants by using methyl jasmonate[J]. Physiology and
Molecular Biology of Plants, 2017, 23(3): 545-556.
[30] Kim Y, Seo C W, Khan A L, et al. Exo-ethylene
application mitigates waterlogging stress in soybean (Glycine max L.)[J]. BMC
plant biology, 2018, 18(1): 1-16.
[31] Wang X, Li F, Chen Z, et al. Proteomic analysis reveals the effects
of melatonin on soybean root tips under flooding stress[J]. Journal of
Proteomics, 2021, 232: 104064.